Selon certaines études, des dépôts d’amyloïde transthyrétine (ATTR) sont retrouvés à l’autopsie chez près de 25 % des hommes de plus de 80 ans, mais ces dépôts ne sont pas toujours symptomatiques. La Haute Autorité de Santé estime le nombre de nouveaux cas en France à 700 par an (1).
Longtemps considérée comme rare, l’amylose cardiaque est aujourd’hui mieux identifiée. Pourtant, elle reste encore sous-diagnostiquée, notamment chez les sujets présentant une insuffisance cardiaque inexpliquée.
Cet article vise à sensibiliser les professionnels de santé à leur rôle clé dans le dépistage de cette maladie auprès des personnes âgées.
Pourquoi détecter l’amylose cardiaque précocement ?
L’amylose cardiaque est un dépôt de protéines anormales dans le muscle cardiaque. Cette accumulation entraîne un épaississement et une rigidité du myocarde pouvant évoluer vers une insuffisance cardiaque.
Santé Publique France estime que 10 % des personnes âgées de 70 ans ou plus sont atteints d’insuffisance cardiaque, et que chaque année près de 70 000 décès y sont associés (2). Parmi ces décès, on retrouve les 25 % des hommes de plus de 80 ans atteints d’amylose.
Les principales formes d’amylose
Il existe différentes formes d’amylose, dont deux principales :
- L’amylose AL (ou amylose à chaînes légères) : un trouble des plasmocytes produisant des chaînes légères d’immunoglobulines anormales.
- L’amylose ATTR (ou amylose à transthyrétine) : une anomalie de la transthyrétine d’origine héréditaire (ATTRh) ou liée au vieillissement (ATTRwt). Cette dernière, dite sauvage, est souvent sous-diagnostiquée dû à ses similitudes avec d’autres cardiomyopathies.
| Type d’amylose | Dépôts | Sources | Organes atteints | Âge moyen au diagnostic |
|---|---|---|---|---|
| Amylose AL | Chaînes légères | Moelle osseuse | Cœur, rein, foie, système nerveux | 67 ans |
| Amylose ATTRh (Héréditaire) | Transthyrétine mutée | Foie | Cœur, système nerveux | 25% : 30 ans 75% : +50 ans |
| Amylose ATTRwt (« Sénile ») | Transthyrétine non mutée | Foie | Cœur | 78 ans |
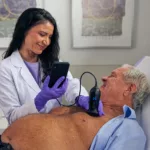
Comment diagnostiquer l’amylose cardiaque ?
Les professionnels de santé jouent un rôle clé dans le dépistage de l’amylose cardiaque. Parmi les signes cliniques évocateurs on retrouve : la fatigue, la prise de poids ou encore des œdèmes aux membres inférieurs. Comme les patients atteints d’amylose sont pour la plus part âgés, ces symptômes passent souvent inaperçus. Il peut donc s’écouler un délai important entre les premiers signes et le diagnostic.
Toutefois, la temporalité de l’apparition de ces symptômes peut être un indice clé pour mettre le praticien sur la piste de cette pathologie. Selon le Protocole National de Diagnostic et de Soins (PNDS), en l’absence de traitement et de suivi adéquat, le pronostic de l’amylose cardiaque s’aggrave considérablement. Sans prise en charge, la survie moyenne est d’environ 6 mois pour les amyloses AL et de quelques années pour les amyloses ATTR.
Pronostic et délais de diagnostic
AMYLOSE AL
Une survie moyenne de 6 mois après le diagnostic cardiaque sans traitement.
Un délai moyen de prise en charge entre les premiers symptômes et le diagnostic de 2 ans (3).
AMYLOSE ATTR
Une survie moyenne de 2 à 4 ans après le diagnostic cardiaque sans traitement.
Un délai moyen de prise en charge entre les premiers symptômes et le diagnostic de 3 à 4 ans en cas d’ATRRwt et 2 à 6 ans en cas d’ATTRh (3).
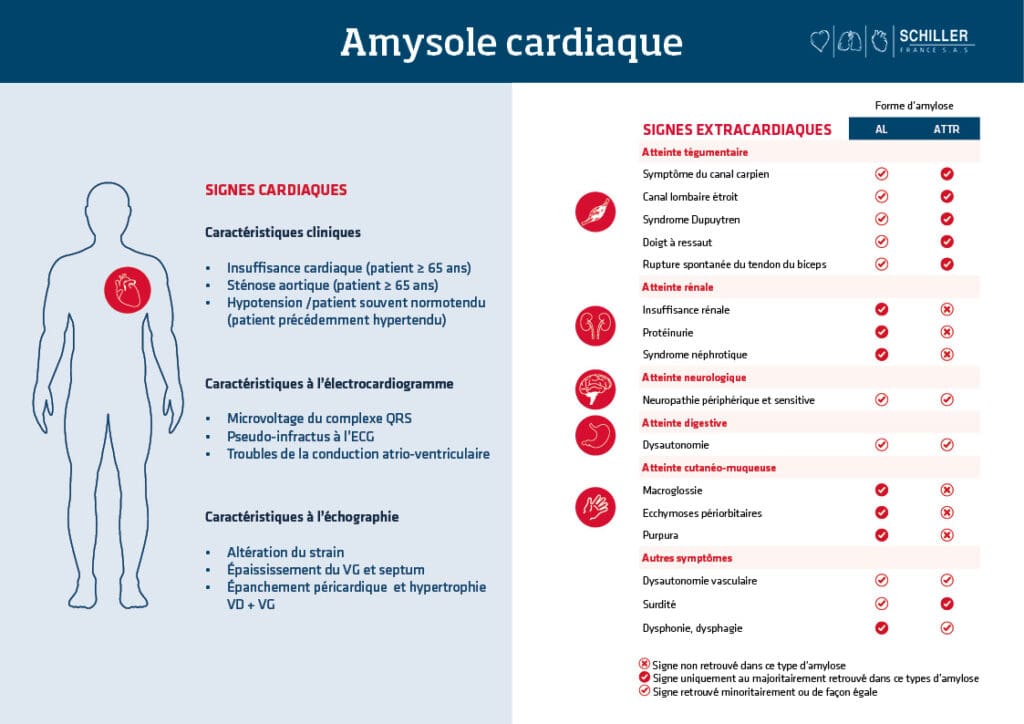
D’autres signes cardiaques et extracardiaques peuvent également orienter le praticien. Pour cela, il est important de réaliser un examen clinique et d’évaluer l’état de santé du cœur du patient à plusieurs niveaux :
- En mesurant l’activité électrique du cœur avec un ECG : pour évaluer les anomalies cardiaques tels qu’un microvoltage des QRS, des pseudo-ondes Q, des QRS fragmentés ou encore des troubles de la conduction à l’étage auriculo-ventriculaire (BAV), classiquement décrits dans les amyloses.
- En observant la morphologie du cœur grâce à une échocardiographie : pour rechercher un épaississement myocardique. Un aspect granité et scintillant du myocarde est fréquent mais non spécifique de l’amylose. La présence de la triade hypertrophie ventriculaire droite et gauche et épanchement péricardique est évocatrice d’amylose mais dans une forme tardive. Si nécessaire, une IRM cardiaque peut être réalisée en complément.
D’autres examens complémentaires seront à réaliser pour confirmer le diagnostic. À savoir, une scintigraphie osseuse et un bilan immunologique. Si ces derniers ne permettent pas de conclure à la présence d’amyloïdes, une biopsie au niveau des tissus graisseux sous cutané ou des glandes salivaires permettra de poser un diagnostic.